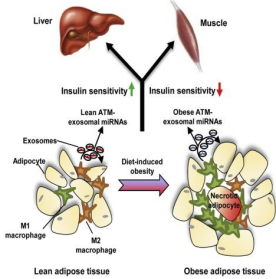
脂肪组织巨噬细胞来源的外泌体miRNA可在体内和体外调节胰岛素敏感性
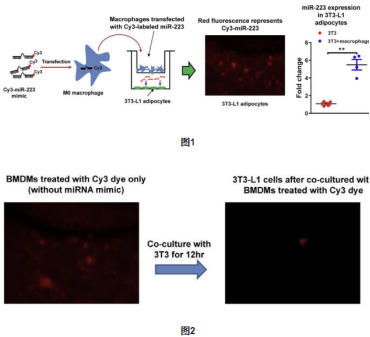
鉴定巨噬细胞能否分泌miRNA:
(1)小室实验
用于证明外泌体从供体细胞释放后,能到达受体细胞,且外泌体以及它体内的货物均能被受体细胞吸收。将Cy3标记miR-233 mimic的转染进骨髓源性巨噬细胞(BMDMS),然后培养于Transwell的上室,下室是不表达Cy3标签的3T3-L1脂肪细胞。共培养12h后,在下室中观察得红色荧光的Cy3-miR-233,是共培养前的6倍,表明这两种细胞间存在一种介质起了运输miRNA的作用(图1)。在对照实验中,我们用Cy3单独(不与miR-223结合)处理BMDMs,在与这些BMDM共培养12小时后,发现这种荧光染料在BMDMs中的出现可忽略不计,在3T3-L1脂肪细胞中没有染料出现(图2)。因此,认为巨噬细胞可以分泌细胞外miRNA,它们被摄取到脂肪细胞中。
鉴定ATM能否分泌外泌体:
为了确认脂肪组织巨噬细胞(ATM)是否可以外泌体,从肥胖野生型小鼠的内脏脂肪组织(VAT)中分离出脂肪组织巨噬细胞(ATM)(CD11b+F4/80+),并培养72小时,电子显微镜(图4)和纳米观察分析(图5)显示,通过超速离心分离的颗粒含有丰富的ATM分泌的胞外小泡,其直径为30-100 nm。这些EV的密度梯度超速离心分析证实,它们主要由Exos组成,通过外体特异性蛋白标记物TSG101、syntenin1、CD63等的表达得到证明,主要以图6表示。
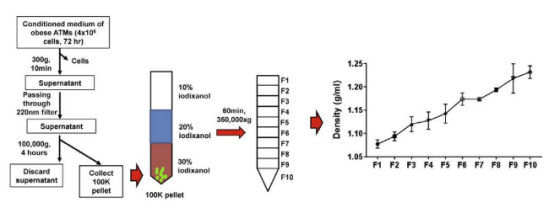
图3. 超速离心分离外泌体
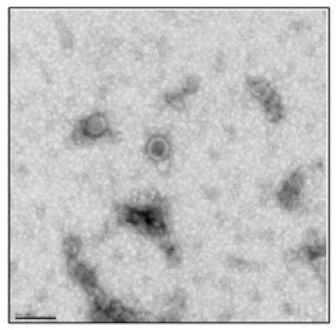
图4.电镜观察外泌体**杯状囊膜结构
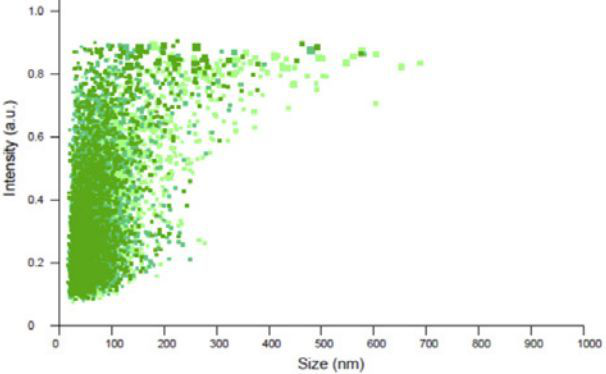
图5.NTA分析外泌体的粒径和浓度表征
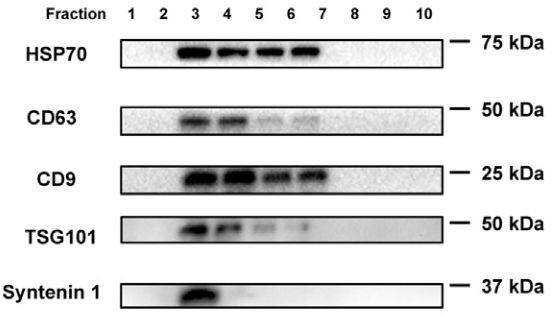
图6.Westernblot鉴定TSG101等外泌体蛋白标志物
产品供应:
胞外囊泡/细胞微粒/微囊泡/外泌体/EVs/exosomes
41860种蛋白质、2838种microRNA、3408种mRNA
外泌体中含RAB4, RAB5和 RAB11,RAB7 和 RAB9
热休克蛋白家族((HSP60, HSP70, HSPA5, CCT2 和HSP90
上述产品仅用于科研,不可用于人体试验!
wyf 01.11




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询